Peptidoak aminoazido anitzek osatutako konposatu klaseak dira, lotura peptidoen bidez. Bizi izaki bizidunetan nonahiko dira. Orain arte, izaki bizidunetan hamarnaka peptido aurkitu dira. Peptidoak funtsezkoa da hainbat sistemen, organo, ehunen eta zelulen jarduera funtzionalak arautzeko eta bizitzako jardueretan, eta askotan analisi funtzionalean, antigorputzak, drogen garapena eta bestelako eremuak erabiltzen dira. Bioteknologia eta peptido sintesiaren teknologia garatuz gero, gero eta peptido gehiago garatu eta aplikatu dira klinikan.
Aldaketa peptido ugari daude. Aldaketa eta prozesuaren aldaketetan banatu daitezke (eratorritako aminoazidoen aldaketa) eta N-terminalaren aldaketa erabiliz, C-terminalaren aldaketa, alboko aldaketa, aminoazidoen aldaketa, eskeletoa eta abar (1. irudia) (1. irudia). Katearen egitura nagusiak edo kate-kate taldeak aldatzeko modu garrantzitsu gisa, ur-disolbagarritasun fisikoak eta kimikoak aldatzeko modu eraginkorrean alda daiteke, biblio biologikoa aldatu, immunogenizitatea desagerrarazteko, paper honetan, eta abar.
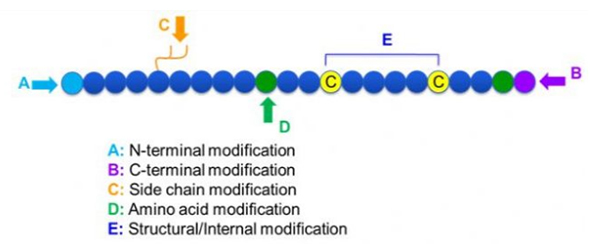
1. Ziklina
Peptido ziklikoek biomedikuntzan aplikazio ugari dituzte, eta jarduera biologikoa duten peptido natural asko peptido ziklikoak dira. Peptido ziklikoak peptido linealak baino zurrunagoak direlako, digestio-sistemarekiko oso erresistenteak direlako, digestio-euskarrian bizi daitezke eta xede-hartzaileentzako afinitate sendoagoa erakutsi dezakete. Txikia da peptido ziklikoak sintetizatzeko moduko modurik gehien, batez ere hezurdura estruktural handia duten peptidoetarako. Txirrindulazio moduan, alboko kate-kate motan, terminal - alboko kate mota, terminal mota (amaiera motaren amaiera) banatu daiteke.
(1) Sidechain-to-Sidechain
Alboko katearentzako albo-kate mota ohikoena cysteine hondakinen arteko desplazamendua da. Zizlizazio hau kenduta dauden zisteinezko hondakin pare batek aurkezten du eta gero hondamendi bonuak eratzeko oxidatu dira. Sintesi polikulikoa Sulfhydryl Babes Taldeak selektiboak kentzea lortu daiteke. Ziklina disolbatzaile osteko disolbatzaile batean edo desbideratze aurreko erretxin batean egin daiteke. Erretxinetan ziklizazioa disolbatzaileen ziklizazioa baino eraginkorragoa izan daiteke, erretxinetan peptidoek ez baitute erraz moldatzen Cyclified Conformazioak. Bigarren mailako katearen ziklizazio mota bat da, azido aspentiko edo azido glutamikoaren hondakinen eta aminoazidoaren oinarriaren arteko amida egitura bat da, eta horrek alboko katearen babes-taldeak polipeptidotik ez du erretxinetik edo disoziazioaren ondoren modu selektiboan kentzeko gai izan behar du. Alboko katearen hirugarren katearen ziklizazioa tirosina edo p-hydroxyphenylglycine diphenyl etekaren eraketa da. Produktu naturaletan ziklizazio mota hau produktu mikrobioetan aurkitzen da eta ziklizazio produktuek sendagai balioa dute maiz. Konposatu horiek prestatzeak erreakzio baldintza bakarrak behar ditu, beraz, ez dira maiz erabiltzen ohiko peptidoen sintesian.

(2) terminal-to-sidechain
Terminal-albo-katearen ziklizazioak normalean C-terminala da Lysine edo Ornithine alboko katearen amino taldearekin edo N-Terminal azido aspentikoarekin edo azido glutamikoko katearekin. Polypeptide beste ziklizazio bat da C terminalaren eta serinearen edo threonine alboko kateen arteko loturak osatuz.
(3) terminala edo buruko buztana mota
Kate polipportidoak disolbatzaile batean ebaki edo erretxina batean konpondu daitezke, alboko katearen ziklizazioaren bidez. Peptidoen kontzentrazio baxuak disolbatzaileen zentralean erabili behar dira peptidoen oligomerizazioa ekiditeko. Buruko buztana sintetikoko polipportaren errendimendua, polipeptide katearen sekuentziaren araberakoa da. Hori dela eta, peptido ziklikoak eskala handian prestatu aurretik, lehenik eta behin kateatutako kateatutako peptidoen liburutegia sortu beharko litzateke, eta ondoren ziklizazioa emaitza onenekin sekuentzia aurkitzeko.
2. N-metilazioa
N-metilazioa jatorriz peptido naturaletan gertatzen da eta peptido sintesian sartzen da hidrogeno bonuen eraketa ekiditeko, eta, horrela, biodegradazioarekiko erresistenteagoak dira. N-metilatutako aminoazido deribatuak erabiliz peptidoen sintesia da metodo garrantzitsuena. Horrez gain, Mitsunobu N- (2-Nitrobenzenen sulfonyl kloruroa) erretxina-erretxina bitartekoak ere erabil daitezke metanola. Metodo hau n-metilatutako aminoazidoak dituzten peptido peptido ziklikoak prestatzeko erabili da.
3. fosforatzea
Fosforilazioa naturaren post-translazio aldaketarik ohikoenetako bat da. Giza zeluletan, proteinen% 30 baino gehiago fosforoak dira. Fosforilazioa, batez ere fosforilazio itzulgarria, zelula prozesu asko kontrolatzeko eginkizun garrantzitsua du, hala nola, seinale transdukzioa, gene adierazpena, zelula zikloa eta zitoskeletoko araudia eta apoptosia.
Fosforilazioa aminoazidoen hondakinen ugaritan ikus daiteke, baina fosforilazioaren helburu ohikoenak serine, threonine eta tirosina hondakinak dira. Fosfotiorosina, fosfothroonina eta fosfoserina deribatuak siroan zehar peptidoetan sartu daitezke edo peptido sintesiaren ondoren eratu dira. Phosforylation selektiboa serine, threonine eta tirosinaren hondakinak erabiliz lor daitezke babes-taldeak modu selektibitateak kentzen dituztenak. Fosforoen erreaktibo batzuek azido fosforikoko taldeak ere aurkeztu ditzakete Polypeptide-n argitaratuz. Azken urteotan, Lysine-ren gunea berariazko fosforilazioa lortu da kimikoki selutificatzaile fosfitoa erreakzioa erabiliz (3. irudia).

4. Myristoylation eta palmitoylation
N-terminalaren akatatzeak gantz azidoekin, peptidoak edo proteinak ahalbidetzen ditu zelulen mintzekin lotzeko. N-Terminal-en sekuentzia mistikoek SRC familiako proteina kinakseak eta alderantzizko transkriptase GAQ proteinak ahalbidetzen dituzte zelulen mintzetara lotzeko. Azido myristikoa erretxina-polipulazioaren N-Terminalarekin lotuta zegoen akoplamendu erreakzio estandarrak erabiliz, eta emaitza lipopeptideak baldintza estandarren azpian dizelatu eta RP-HPLC-k araztu zuen.
5. glukosilazioa
Vancomicina eta Teicolanina bezalako glikopeptidoak antibiotiko garrantzitsuak dira drogak erresistenteak diren bakterioen infekzioak tratatzeko, eta beste glukopeptido batzuk erabiltzen dira sistema immunologikoa suspertzeko. Gainera, mikrobioen antigeno asko glukosilatuak dira, esangura handia du infekzioaren eragin terapeutikoa hobetzeko glikopeptidoak aztertzeko. Bestalde, tumore zelulen zelulen mintzaren inguruko proteinak glukosilazio anormalak erakusten dituela aurkitu da, eta horrek glikopeptidoak eginkizun garrantzitsua du minbizia eta tumorearen defentsa immunologikoko ikerketan. Glikopeptidoak FMOC / T-BU metodoaren bidez prestatzen dira. Glycosylated hondakinak, hala nola, threonine eta serine, maiz sartzen dira PentAfluorofenol Ester-ek FMocs aktibatutako FMOCS-ek aminoazido glikosilatuak babesteko.
6. Isoprene
Isopentadienylation C-Terminaletik gertu dagoen alboko katearen inguruko zisteen hondakinetan gertatzen da. Proteinen isoprenoak zelulen mintzaren afinitatea hobetu dezake eta proteina-proteinen elkarrekintza eratu dezake. Isopentadienatutako proteinak tirosina fosfatasa, gtase txikia, cochaperone molekulak, lamina nuklearra eta proteina zentromerikoak dira. Isoprenoko polipportidoak isoprenoa erretxinetan erabiliz presta daiteke edo zisteinazko deribatuak sartuz.
7. Polietileno glikola (PEG) Aldaketa
PEG aldatzea proteina egonkortasun hidrolitikoa, biodibributua eta peptidoaren disolbagarritasuna hobetzeko erabil daiteke. PEG kateak peptidoei sartzeak propietate farmakologikoak hobetu ditzake eta entzima proteolitikoen peptidoen hidrolisia ere inhibitu dezake. PEG Peptides-ek kapilako atal glomerularraren ataletan peptido arruntak baino errazago pasatzen ditu, giltzurruneko garbiketa asko murriztuz. Vivoko PEG peptidoen erdibizko bizitza aktibo hedatuaren ondorioz, tratamendu maila normala dosi txikiagoekin eta gutxiagotan peptidoen drogekin mantendu daiteke. Hala ere, Peg Aldaketak ere efektu negatiboak ditu. Peg kopuru handiek entzima peptidoa degradatzea eragozten dute eta peptidoaren xede hartzaileari loteslea murriztea. Baina Peg Peptides 'afinitate baxua bizitza erdiko farmakokinetiko luzeagoarekin konpentsatzen da, eta gorputza luzeago egonez gero, peg peptidoek xede-ehunetan xurgatzeko probabilitate handiagoa dute. Hori dela eta, PEG polimeroen zehaztapenak emaitza optimoak optimizatu beharko lirateke. Bestalde, peg peptidoak gibelean metatzen dira giltzurruneko garbiketa murriztua dela eta, sindrome makromolekularra sortuz. Hori dela eta, Peg aldaketak arretaz diseinatu behar dira peptidoak drogak probatzeko erabiltzen direnean.

Peg aldatzaileen aldaketaren ohiko taldeak honela laburbildu daitezke: -NH2 -Nh2, aminomethyl-ch2-nh2, hidroxy-oh, carboxy-cooh, sulfhydryl (maleimidoa) -Sc, succinimide azetatoa -scm, succinimide propionate -spa, n-hydroxysuccinimide -nhs, akrilato-ch2ch2cooh, Aaldehyde -cho (esaterako, propional-Ald, Butyrald), Oinarri akrilikoa (-CryLate-ACRL), azido-azidoa, biotiniloa, fluorescein, glutaryl -ga, akrilatoa Hidrazida, Alkyne-Alkyne, P-Toluenesulfonatoa -ots, succinimide succinate -ss eta abar azido karboxilikoak dituzten deribatuak N-terminal amines edo lisina alboko kateetara lotu daitezke. Amino-Aktibatutako Peg azido aspartiko edo azido glutamikoko kateetara lotu daiteke. Aktibatutako Peg-ek guztiz kendutako kiste-kateen Mercaptan-era konjugatu daiteke [11]. PEG aldatzaileak jarraibide gisa sailkatzen dira normalean (oharra: MPED Methoxy-Peg, Ch3o- (Ch2ch2o) N-Ch2ch2-Oh):
(1) Kate zuzeneko aldatzailea
MPEG-SC, MPEG-SCM, MPEG-SPA, MPEG-OTS, MPEG-SH, MPEG-ALD, MPEG-BUTYRALD, MPEG-SS
(2) Bifuntzional Peg aldatzailea
Hcoo-Peg-Cooh, NH2-PEG-NH2, Oh-Peg-Cooh, Oh-Peg-NH2, HCl · NH2-PEG-Cooh, Mal-Peg-NHS
(3) adar peg aldatzailea
(MPEG) 2-NHS, (MPEG) 2-ALD (MPEG) 2-NH2, (MPEG) 2-MAL
8. Biotinizazioa
Biotina biziki lotuta egon daiteke avidinarekin edo estremoarekin, eta lotura loteslea lotura kobalentearengandik gertu dago. Biotin-etiketatutako peptidoak immunoasy, histokitokimika eta fluoreszentzian oinarritutako zitometria erabiltzen dira. Antibiodiko antigorputz etiketatuak biotinilatutako peptidoak lotzeko ere erabil daiteke. Biotinen etiketak maiz lisatzeko alboko kateari edo n terminalari atxikitzen zaizkio. 6-azido aminocaproikoa maiz erabiltzen da peptidoen eta biotinen arteko lotura gisa. Bonua malgua da substratuarekin lotuta eta hobeto lotzen da oztopo estetikoaren aurrean.
9. Etiketatze fluoreszentea
Etiketa fluoreszenteak zelula bizidunetan polipeptidoak trazatzeko eta entzimak eta ekintza mekanismoak aztertzeko erabil daiteke. Tryptophan (Trp) fluoreszentea da, beraz, berezko etiketarako erabil daiteke. Triptofanoaren emisioen espektroa ingurune periferikoaren araberakoa da eta disolbatzaile polaritatea gutxitzen da, peptidoaren egitura eta hartzailearen loteslea detektatzeko erabilgarria den jabetza da. Tryptophan fluoreszentzia azido aspartiko eta azido glutamikoen protonizatuen bidez itzali daiteke, eta horrek bere erabilera mugatu dezake. Dansilloko kloruroaren taldea (Dansil) oso fluoreszentea da amino talde bati lotuta dagoenean eta askotan aminoazido edo proteinen etiketa fluoreszente gisa erabiltzen da.
Fluoreszentzia Erresonantzia Energia Bihurketa (Fret) erabilgarria da entzima ikasketetarako. Fret aplikatzen denean, substratu polipeptideak normalean fluoreszentzia-etiketatzeko taldea eta fluoreszentzia-taldea biltzen du. Talde fluoreszenteak etiketatuarengandik ateratzen dira fotoi ez-transferentziaren bidez. Peptidoa kasuan kasuko entzimatik banatzen denean, etiketatze taldeak fluoreszentzia igortzen du.
10. Kaiola polipeptidoak
Kaiola peptidoek babes-talde optikoki aldagarriak dituzte, peptidoa babesten dutenak hartzaileari lotuta. UV erradiazioaren eraginpean dagoenean, peptidoa aktibatuta dago, bere afinitatea hartzaileari leheneratzen. Aktibazio optiko hori denboraren, anplitude edo kokapenaren arabera kontrolatu daitekeelako, kaiola peptidoak zeluletan gertatzen diren erreakzioak aztertzeko erabil daitezke. Kaiolaren polipeptidoetarako gehien erabiltzen diren babes-taldeak 2 nitrobenzil talde dira eta horien eratorriak, sintesia peptidoetan sartu daitezke aminoazidoen deribatu babesgarrien bidez. Garatu diren aminoazidoen deribatuak lisina, zisteina, serine eta tirosina dira. Aspartatu eta glutamatoaren eratorriak, ordea, ez dira normalean erabiltzen ziklizazioaren ondorioz, peptido sintesia eta disoziazioan zehar.
11. Peptido polinantenikoa (mapa)
Peptido motzak normalean ez dira immunitateak eta garraiolarien proteinei lotu behar zaizkie antigorputzak ekoizteko. Peptido polinantenikoa (mapa) Lysine Nuclei-rekin lotutako peptido berdinez osatuta dago, eta horrek ahaltsikako immunogeno altuak berariaz adierazi ditzake eta peptido-garraiolarien koplak prestatzeko erabil daiteke. Mapa polipeptidoak fase solidoaren sintesiaren bidez sintetizatu daitezke maparen erretxinetan. Hala ere, akoplamendu osatu gabeko kate peptidoen kateak erauzi edo ebakitzen dira adar batzuen gainean eta, beraz, ez ditu jatorrizko maparen propietateak erakusten. Alternatiba gisa, peptidoak bereizita prestatu eta garbitu daitezke eta ondoren mapan lotu. Peptidoaren muina atxikitako sekuentzia peptidoaren sekuentzia ondo zehaztuta dago eta erraz bereizten da espektrometria masiboa.
Bukaera
Peptidoaren aldaketa peptidoak diseinatzeko bide garrantzitsua da. Kimikoki eraldatutako peptidoek ezin dute jarduera biologiko altua mantendu, baita immunogenismoaren eta toxikotasunaren eragozpenak ere modu eraginkorrean saihestea. Aldi berean, aldaketa kimikoek propietate bikain batzuekin peptidoak hornitu ditzakete. Azken urteotan, polipportidoen aldizkariaren aldaketarako C-H aktibazio metodoa azkar garatu da eta emaitza garrantzitsu asko lortu dira.
Ordua: 03-07-07
