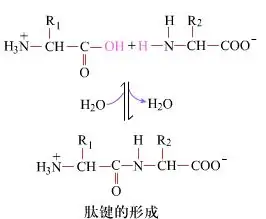
Azalean, lotura peptidoen eraketa, dipettidoak errendimendua, prozesu kimiko sinplea da. Horrek esan nahi du aminoazidoen bi osagaiak lotura peptido baten bidez lotuta daudela, deshidratatuta egon bitartean.
Peptido Bonuen eraketa aminoazido baten aktibazioa da erreakzio baldintza arinen azpian. (A) carboxyl moistión, bigarren aminoazidoa (b) aktibatutako karboxiliko nukleofilikoen ondorioz, eta ondoren dipeptide (A-B) osatzen dute. "Carboxyl osagaia (a) babestuta ez badago, ezin da kontrol peptidoaren eraketa kontrolatu." Peptido linealak eta ziklikoak bezalako produktuak A-B konposatu xedeekin nahastu daitezke. Hori dela eta, lotura peptidoaren eraketan parte hartzen ez duten talde funtzional guztiek aldi baterako itzul daitekeen moduan babestu behar dira peptido sintesian zehar.
Beraz, peptido sintesia - lotura peptido bakoitzaren eraketa - hiru urratsak dakartza.
Lehen urratsa babestea behar duten aminoazido batzuk prestatzea da, eta aminoazidoen egitura zwitterionikoa ez da gehiago existitzen.
Bigarren urratsa bi urratseko erreakzioa da lotura peptidoak osatzeko, eta bertan N-Protected Aminoazideko karboxikoen taldea bitarteko aktiboarekin aktibatzen da lehenengo eta gero lotura peptidoa eratzen da. Akoplatutako erreakzio hau urrats bakarreko erreakzio gisa edo sekuentziako bi erreakzio gisa gerta daiteke.
Hirugarren urratsa babes-oinarria kentzea edo erabateko kentzea da. Kendu guztiak kentzea peptido kate guztiak muntatu ondoren bakarrik gerta daitezke, babes-taldeak kentzea ere beharrezkoa da peptido sintesia jarraitzeko.
10 aminoazido (ser, thr, tyr, tyr, asp, glu, argiak, argiak, bere, sec eta CYS) alboko kate talde funtzionalak dituzte, babes selektiboa eskatzen dutenak, peptido sintesia konplikatuagoa izatea. Babes aldi baterako eta erdi iraunkorrak diren oinarriak bereiztu behar dira selektibitatearen eskakizun desberdinengatik. Aldi baterako Babes taldeak hurrengo urratsean erabiltzen dira aminoazidoen edo karboxilen talde funtzionalen aldi baterako babesa islatzeko. Babes-talde erdi iraunkorrak kentzen dira jada eratutako peptidoaren fidantzak edo aminoazido alboko kateak oztopatu gabe, batzuetan sintesi garaian.
"Egokiena, karboxilaren osagaiak aktibatzea eta ondorengo bonuak (akoplamendu erreakzioak) azkarrak izan beharko lirateke, arrazakeriarik gabe edo produktuen eraketarik gabe, eta erreaktibo molarak eman behar dira etekin altuak lortzeko." Zoritxarrez, akoplamendu kimikoko metodo kimikoetako batek ez du baldintza horiek betetzen, eta gutxi dira sintesi praktikoetarako egokiak.
Peptidoaren sintesian, hainbat erreakzioetan parte hartzen duten talde funtzionalak normalean eskuzko zentroarekin lotuta daude, glicina salbuespen bakarra izanik, eta biraketa arriskua dago.
Peptidoaren sintesi zikloaren azken urratsa babes-talde guztiak kentzea da. Babes taldeak kentzea garrantzitsua da peptido-katearen luzapenerako, dipeptide sintesian babes osoa kentzeko eskakizunaz gain. Estrategia sintetikoak arretaz planifikatu behar dira. Aukera estrategikoaren arabera, n-k α-amino edo carboxyl babesteko taldeak modu selektiboan kendu ditzake. "Estrategia" terminoak aminoazido indibidualen kondentsazio erreakzioen sekuentzia aipatzen du. Orokorrean, desberdina da pixkanaka sintesia eta zatiken kondentsazioaren artean. Peptido sintesia ("sintesi konbentzionala" izenez ere ezaguna da soluzioan. Gehienetan, peptido katearen luzapena pixkanaka luzatzea kate peptidoaren bidez soilik sintetizatu daiteke zati laburragoak sintetizatzeko. Peptido luzeagoak sintetizatzeko, xede molekulak zatitxo egokiak segmentatu behar dira eta C termino-ren desberdintasun maila gutxitu dezaketela zehaztu behar da. Banakako zatiak pixkanaka muntatu ondoren, xede konposatua batu egingo da. Peptido sintesiaren estrategiak babes-zati onena eta egokiena hautatzea dakar.
Ordua: 02/07-07